臨床工学技士のナキです。
今回は、実際に末梢血幹細胞採取に従事している臨床工学技士、臨床検査技師や看護師さんに向けて、末梢血幹細胞採取に必要な知識をまとめてみました。
目次
末梢血幹細胞採取とは?
末梢血幹細胞採取とは、G-CSFなどで骨髄内の造血幹細胞を末梢血へ動員したうえで、Spectra Optiaという装置を用いて、循環血から造血幹細胞を分離・採取することです。
採取した細胞は、自家/同種造血幹細胞移植に用いられます。
参考:Stem Cell Transplants in Cancer Treatment
採取手順と装置設定【Spectra Optia】
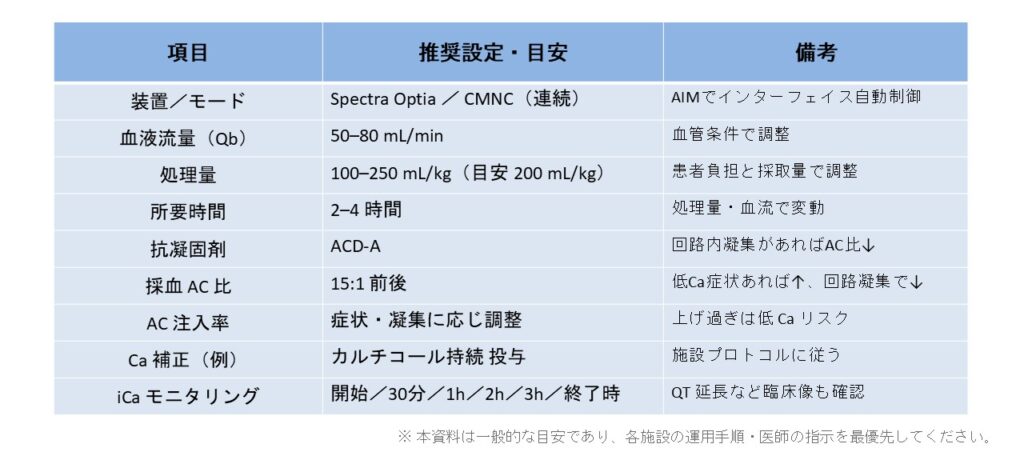
ここでは、Spectra Optiaの実際の設定項目の解説をしていきます。
基本パラメータ
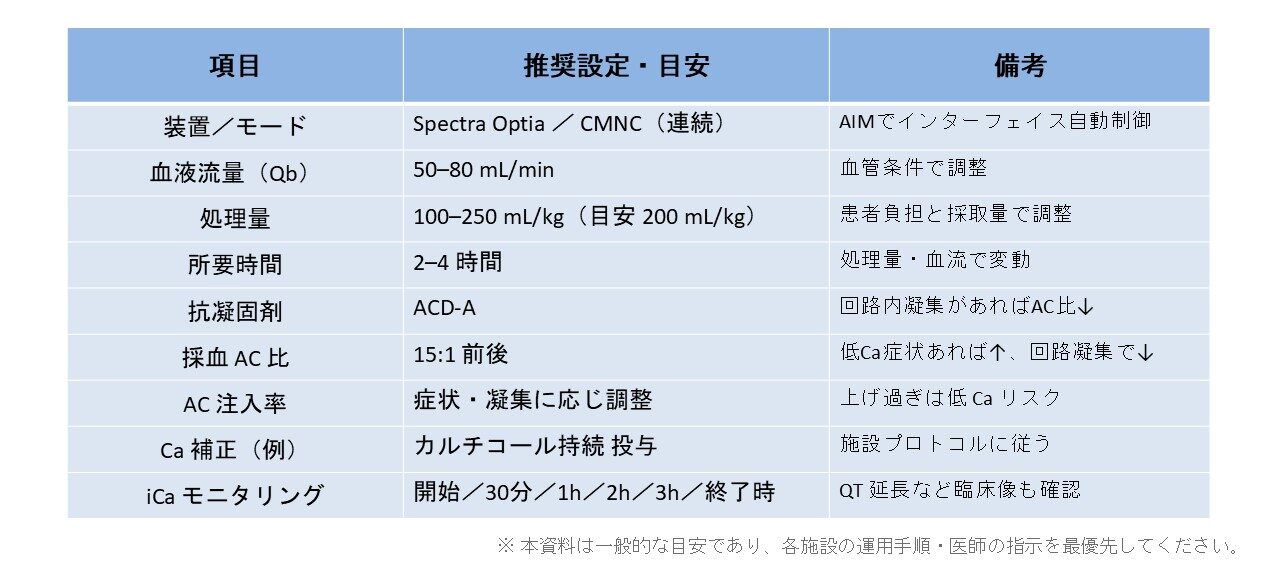
上記はあくまで目安です。
AIMとは?
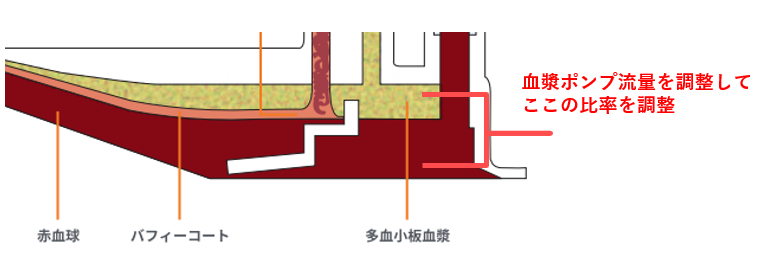
光学センサで「採取ポートを通る細胞濃度」を常時監視し、血漿ポンプの流量を自動で調整して分離層(インターフェイス)を安定させる制御システムのことです。
遠心分離でできる層(血球層と血漿層)の位置を、この血漿ポンプの流量を調整することで、採取ポートを流れる細胞濃度を安定させています。
参考:Spectra Optia Operator’s Manual
インターフェイスとは?
インターフェイスとは、遠心分離チャネル内で形成される層の「境目」のことです。具体的には、赤血球層と血漿層のあいだに生じるバフィーコート(白血球・血小板が集まる薄い層)付近の境界のことです。ここをどの位置に保つかで「どの成分が採取ポートに流れ込むか」が左右されます。
AIMとインターフェイスの関係
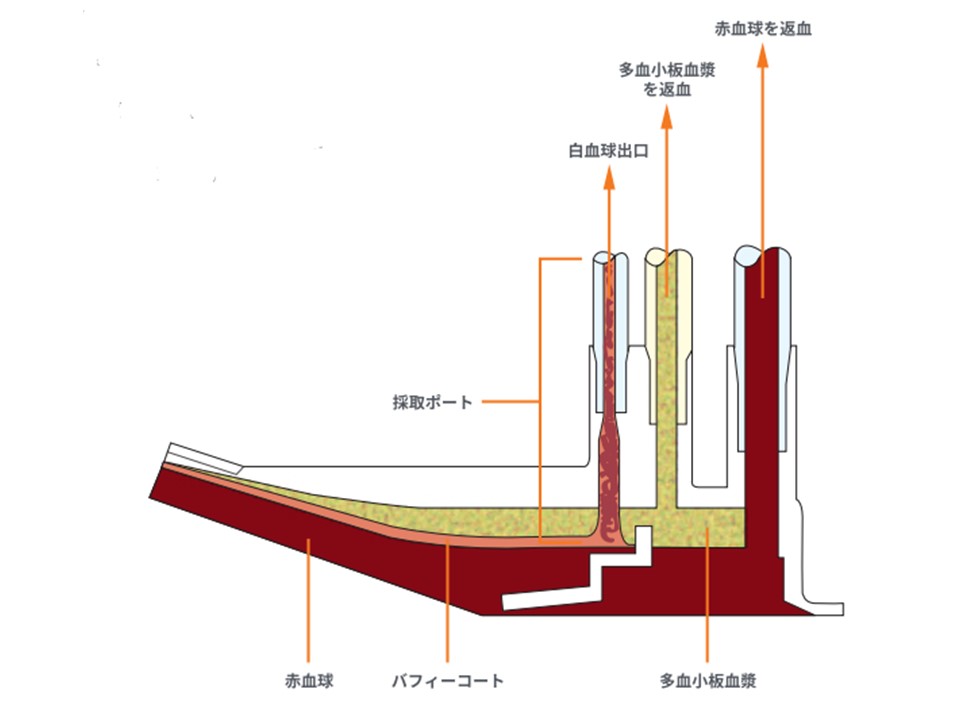
すなわち、インターフェイス=チャネル内の境界層(主に血漿/赤血球)のこと。AIMはここを光学センサで監視し、血漿ポンプの流量で微調整して、目的成分の採取を狙っているということです。
バフィーコート
バフィーコートとは、遠心力により血漿と赤血球の間にできる白色の薄い層のことです。主に白血球(単核球・顆粒球)と血小板が集まった部分です。
末梢血幹細胞採取では、このバフィーコートを狙うことで、目的の造血幹細胞を採取することができます。
採取プリファレンス(CP)
採取プリファレンス(CP)は、AIMが採取ポートを流れる細胞濃度の目標値として参照する値です。
CMNCではCP=50がデフォルトの設定となっており、状況に応じてCPを上下させます。
例えばCPを下げた場合、赤血球層寄りに狙いをつけて採取することになり、採取する細胞濃度を上げること(採取バッグは赤みが強くなります)ができますが、RBCの混注に注意が必要です。
逆にCPを上げる場合、血漿層側寄りに狙いをつけて採取することになるため細胞濃度は減ります(採取バッグの赤みは薄くなります)。
ようするに、CPはバフィーコートのどれくらいの位置で採取するかの目標値です。
OptiaのTBV(Total Blood Volume)とは?
TBV=推定総循環血液量です。
Optiaは性別・身長・体重からTBVを自動計算し、
①Run target「TBV processed(例:2.0×)」
②AC注入上限(mL/分/L-TBV)
の基準に用いられています。
体重25kg未満は自動計算されないため、手計算→手入力が必要です。
TBVが使われる主な場面
| 用途 | 概要 | 目安/範囲 |
|---|---|---|
| Run target:TBV processed | 「患者のTBVの何倍を処理するか」を指定。TBV×を入れると、他のターゲット(時間/処理量)は自動的に0に設定。 | 0.5–5×(手順により既定値あり) |
| AC注入上限 | AC(ACD-A)の安全上限をmL/分/L-TBVで管理。症状や採取状況で調整。 | 推奨上限1.2 mL/分/TBV(状況により1.3–2.5の注意域で調整可) |
| 小児/低TBVの扱い | 25kg未満は装置がTBVを計算しないため、手計算→手入力。流量/AC/プライミングに配慮。 | 最低Inlet 5 mL/分など手順の下限に注意 |
TBVの計算式(Nadler式;目安)
身長 H(m)、体重 W(kg) とすると:
- 男性:
TBV(L) = 0.3669 × H3 + 0.03219 × W + 0.6041 - 女性:
TBV(L) = 0.3561 × H3 + 0.03308 × W + 0.1833
(Optiaは入力した性別・身長・体重からTBVを算出します。必要に応じてTBVボタンで手入力に切替可能)
現場での注意
- 小柄・低TBVでは、AC負荷と体外循環比に注意。
- TBV processedは採取目標(CD34⁺必要量)とアクセス条件に合わせて設定。
参考文献
Terumo BCT. Spectra Optia® Apheresis System Operator’s Manual(TBVの自動計算・手入力、Run target: TBV processed の記載あり)
Terumo BCT. Concepts of Anticoagulant (AC) Management(AC注入上限:~1.2 mL/min/L-TBV ほか)
Terumo BCT. Spectra Optia TPE Procedure Training(weight <25 kg ではTBV自動計算なし)
StatPearls. Physiology, Blood Volume(Nadler式の係数)
Wiley JCA. Safety and performance of the Spectra Optia apheresis system(TBV processed設定の臨床文脈)
疾患別:目標CD34⁺採取量(自家造血幹細胞移植)
単回の自家移植では最低 2×106 CD34⁺/kgを切らないことが大前提です。
目標は疾患ごとにおおむね4–6(多発性骨髄腫)、5(リンパ腫・PCNSL)、≥4.5–5(ALアミロイドーシス)が目安です。将来の再移植なども見据えるなら合計 8–10の確保を検討します。
目安表(×106 CD34⁺/kg)
| 疾患 | 目標 | 最低許容 | 補足 |
|---|---|---|---|
| 多発性骨髄腫(MM) | 4~6 | 2 | 国際骨髄腫ワーキンググループは単回で4~6、将来分まで集めるなら8~10の採取を推奨。 |
| DLBCL/ホジキンリンパ腫(HL) | 5 | 2 | ≧5で発熱性合併症や抗菌薬日数の減少・回復促進の報告多数。 |
| マントル細胞リンパ腫(MCL) | ≥4~5 | 2 | 多くのプロトコールが4以上を目標に設定。 |
| 中枢神経原発リンパ腫(PCNSL) | ~5(標準) | 2 | PCNSLは“量”より移植片の組成の影響も示唆。施設では一般自家造血幹細胞移植と同じ閾値(≧2)を採用しつつ5前後を目安に運用。 |
| ALアミロイドーシス | ≥4.5~5 | 2 | 最新の多施設解析で≧4.5が生着・生存の独立良好因子。 |
※自家造血幹細胞移植の目安です。将来の再移植やCAR-T後の造血回復まで考える場合は、合計 8–10×106/kgの確保も検討します。
※採取量は通常、実体重(kg)基準で算出します。
参考文献
Pasvolsky O. Optimal infused CD34⁺ cell dose in multiple myeloma patients undergoing upfront autologous hematopoietic stem cell transplantation. Blood Cancer Journal. 2024.
EBMT Handbook(Mobilization & Collection). Mobilization and Collection of HSC. EBMT Handbook. 2023/2024.
Scheid C, et al. Using at least 5×106/kg CD34⁺ cells for ASCT reduces febrile complications. Bone Marrow Transplant. 1999.
Hosing C, et al. High-dose chemotherapy and autologous hematopoietic stem cell transplantation. Biol Blood Marrow Transplant. 2008.
Muchtar E, et al. The impact of melphalan schedule and CD34⁺ dose on post-transplant outcomes in AL amyloidosis. Am J Hematol. 2025.
Partanen A, et al. Blood graft and outcome after ASCT in primary CNS lymphoma. Journal of Hematology. 2021.
代表的な合併症と対策
クエン酸反応(低Ca)
抗凝固薬であるACD(クエン酸)がイオン化カルシウムをキレートして、低Ca血症となり、しびれ(口周囲・指先)、筋痙攣、悪心、めまい、重症例ではテタニー不整脈などが起こることがあります。
対応:iCaを経時的に測定、カルチコールの持続投与。AC注入率を下げる。
VVR(血管迷走神経反射)
徐脈・血圧低下・冷汗がみられたら、体位調整・会話で安心させて、輸液などで対応します。
穿刺・血管トラブル
返血圧上昇・脱血不良は安全優先。無理に続けず、仕切り直しも選択肢です。
クエン酸による低Ca症状が出たときの対応(カルチコール8.5%)
症状が出たら「クエン酸流入を下げる(AC比を上げる)」→「カルチコール8.5%でCaをボーラス又は持続投与速度上げる」→「iCaを30–60分ごとに確認」。
予防は少量の持続Ca(開始目安:1.4–1.9 mmol/時)
- 理由:クエン酸はCaをキレートして体内のiCaを下げ、しびれ・悪寒・不整脈などを起こします。
- 根拠:Buchta 2003は1.8 mmol/時のCa持続で症状を約65%減、他研究でも持続投与・予防投与の有用性が示されています。
すぐに行うこと(現場アルゴリズム)
- クエン酸流入を減らす:
AC比を上げる(例:12:1 → 14–16:1)。 - Caを補う(カルチコール8.5%):
- ボーラス(末梢静脈):
10 mLを5–10分で静注(= 約1.95 mmol)。反応が弱ければ追加5–10 mLを検討します。 - 持続投与:開始目安1.8 mmol/時(Buchta 2003)。
※カルチコール8.5%は1 mL=0.195 mmolなので、1.8 ÷ 0.195 ≒ 9–10 mL/時で開始し、症状・iCaで微調整します。
- ボーラス(末梢静脈):
- モニタリング:
iCa(必要に応じてiMgやQT間隔)を30–60分ごとに確認し、持続投与量を1–2 mL/時刻みで増減します。 - 重症(痙攣・著明なQT延長・不整脈):
処置を一時中断・心電図監視のうえ、ボーラスを反復+持続を上乗せし、主治医の管理下で対応します。
カルチコール8.5%の用量換算(覚え書き)
- 含量:1 mLあたりCa 7.85 mg = 0.39 mEq = 0.195 mmol(添付文書)。
- ボーラス:
10 mL=1.95 mmol(症状に応じて追加)。 - 持続投与の計算式:
設定(mL/時) = 目標Ca(mmol/時) ÷ 0.195
例)1.5 mmol/時 → 約7.7 mL/時、1.8 mmol/時 → 約9–10 mL/時。
再燃防止と予防
- 予防的Ca持続(PBSCの長時間採取や再燃例):
1.4–1.9 mmol/時(=7.2–9.7 mL/時)で開始し、症状・iCaで微調整します。 - 経口Caの併用:静注Caに経口Ca飲料を組み合わせると症状頻度が下がる報告があります(RCT/実臨床報告)。
注意点(安全性)
- 強心配糖体(ジギタリス等)併用は禁忌、腎機能・高Caに注意(添付文書)。
- 過補正を避ける:iCaの上がり過ぎ(高Ca)にも注意し、終了後もしばらくモニターします。
- 運転面:ACD-Aの“希釈”ではなく、原則はAC比で調整します。
参考文献
1) Buchta C, et al. Reduction of adverse citrate reactions during autologous large-volume PBPC apheresis by continuous infusion of calcium-gluconate. Transfusion. 2003.
2) Hegde V, et al. Prophylactic low dose continuous calcium infusion during PBSC collections to reduce citrate related toxicity. Transfus Apher Sci. 2016.
3) Bolan CD, et al. Controlled study of citrate effects and response to i.v. calcium during allogeneic PBPC donation. Transfusion. 2002.
4) Fujii K, et al. Effectiveness of supplemental oral calcium drink in preventing citrate-related adverse effects in PBPC collection. Transfus Apher Sci. 2021.
5) Abe M, et al. Oral calcium supplementation versus placebo in mitigating citrate-related hypocalcemia during PBPC apheresis: randomized trial. Hematol Transfus Cell Ther. 2024.
6) Lee G, Arepally GM. Anticoagulation techniques in apheresis: from heparin to citrate. J Clin Apher. 2012.
7) Jo T, et al. Risk analysis of fluctuating hypercalcemia after leukapheresis. Sci Rep. 2023.
8) カルチコール注射液8.5% 添付文書(JAPIC)(PDF)/KEGG医薬品
よくある質問(F&Q)
採取はいつ始めますか?
末梢血CD34+が10〜20/µLの範囲に入ったら開始を検討します。10/µL未満は動員不十分のサインです。
低Ca対策はどうしますか?
クエン酸反応の予防としてCa製剤の持続投与を行います。イオン化Caの確認とAC比の調整をセットで行います。
取れが悪いときの対応は?
初回で目標の1/3未満しか採れない場合は、次回にプラリキサフォル(モゾビル)の追加を検討します。化学療法歴や骨髄抑制も評価します。
採取時間が長引くときの優先順位は?
採取よりも安全を優先します。
患者さんの症状や回路トラブルが続く場合は、採取に固執せずに、翌日に仕切り直して採取することを考慮します。
まとめ
- 開始は末梢血CD34+ 10〜20/µL、目標は2〜5×10^6個/kgが目安です。
- Spectra Optiaの設定はAC 12〜13:1/CP 50前後/から始め、症状と混入で微調整します。
- 低Ca・VVRは予防と早期対応で安全に進めます。CE1/CE2は次回の設定調整に活かします。
※本記事は一般的な目安です。各施設のプロトコール、装置マニュアルに従って運用してください。