こんにちは、臨床工学技士の秋元です。
半透膜を通ることができない物質というのは、水の移動(浸透、浸透圧)を引き起こします。
— 秋元@臨床工学技士 (@akimotoME) May 8, 2021
上記のツイートのとおり、半透膜を通過できない物質というのは水の移動(浸透、浸透圧)を引き起こします。
本記事では、このツイートの意味を深掘りして、浸透圧とはなんなのかを図を多用してわかりやすく解説しています。
拡散についてはなんとなく、コーヒーにミルクをたらせば、徐々にコーヒー全体にミルクが広がっていく、すなわち「拡散」がイメージできやすいと思います。しかし、「浸透」といわれると、なんだかイメージがつきにくいと思います。
しかし、本質的には拡散と浸透は「同じ」であることが本記事を読むとわかります。
目次
浸透圧とはなにかをわかりやすく解説してみた
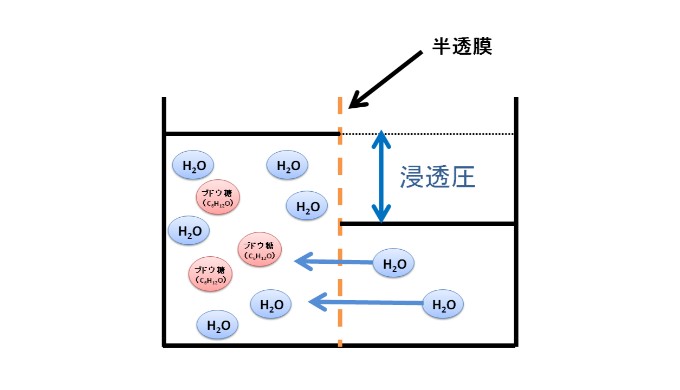
- 浸透圧:上の図において、右側の液面と左側の液面の差に相当する圧力のこと。いい換えると、浸透圧とは水を引っ張る力ともいえる。
上の図において、右側の液面と左側の液面の高さの差に相当する圧力を、浸透圧といいます。
ただ、これだけだと何のことだかわからないと思いますので、順を追ってわかりやすく解説していきます。
上の図のように、半透膜を通過できない分子(例:ブドウ糖)があると、半透膜を通過できる分子(例:水)は、拡散によって全体の濃度を均一にしようとします。
その結果、水分子は半透膜をとおって、左側の溶液に移動するので、左側の溶液の液面が上昇(左側の溶液の水量が増加)します。
しかし、左側の液面と右側の液面の差に相当する圧力が水を押し戻そうとする力が発生します。そのため、ある一定のところで、左側の液面の上昇はとまります。
この左側の液面と右側の液面の高さの差に相当する圧力を、浸透圧といいます。
ようするに、左側の溶液のほうがブドウ糖がある分、濃度が高いので、水を引き込む力(浸透圧)があるということです。
それでは次に、浸透圧をより詳しく理解するために「拡散」と「浸透」の違いについて解説します。
拡散とは
拡散とは、熱運動している粒子(原子、分子、イオンなど)が、周囲の粒子と衝突しながら自然にゆっくりと空間全体に広がっていく現象のことです。
熱運動とは、粒子(原子、分子、イオンなど)が、温度に応じていろんな「速さ」と「方向」で絶えず運動していることです。温度が高いほど、熱運動のエネルギーは大きくなります。
ようするに、濃度が不均一な状態にある場合、時間とともに濃度が均一な状態になっていくということです。この物質の濃度が均一になる過程を拡散といいます。
浸透とは

浸透とは、熱運動している溶媒(溶媒とは溶質を溶かしている液体のことで、水のことが多い)粒子が、半透膜を通って拡散する現象のことです。
ようするに、浸透とは半透膜を介した溶媒(例:水)の拡散現象だということです。
そういう意味でいうと、拡散と浸透は、本質的には同じ現象です。
拡散と浸透の違い
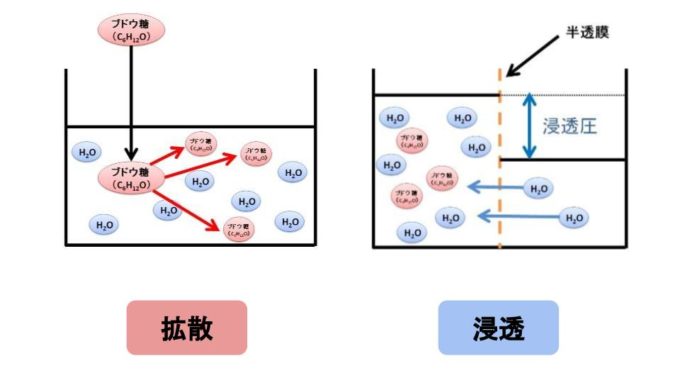
- 拡散とは:熱運動している粒子(原子、分子、イオンなど)が、周囲の粒子と衝突しながら自然にゆっくりと空間全体に広がっていく現象のことです。
- 浸透とは:熱運動している溶媒(溶媒とは溶質を溶かしている液体のことで、水のことが多い)粒子が、半透膜を通って拡散する現象のことです。
拡散とは、熱運動している粒子(原子、分子、イオンなど)が、周囲の粒子と衝突しながら自然にゆっくりと空間全体に広がっていく現象のことです。
一方、浸透とは熱運動している溶媒(溶媒とは溶質を溶かしている液体のことで、水のことが多い)粒子が、半透膜を通って拡散する現象のことです。
ようするに、浸透とは半透膜を介した溶媒(例:水)の拡散現象だということです。
そういう意味でいうと、拡散と浸透は、本質的には同じ現象です。
浸透圧とは

- 浸透圧:上の図において、左側の液面と右側の液面の差に相当する圧力のこと
内容を復習します。
上の図のように、半透膜を通過できない分子(例:ブドウ糖)があると、半透膜を通過できる分子(例:水)は、拡散によって全体の濃度を均一にしようとします。
その結果、水分子は半透膜をとおって、左側の溶液に移動するので、左側の溶液の液面が上昇します。
しかし、左側の液面と右側の液面の差に相当する圧力が水を押し戻す力が発生します。そのため、ある一定のところで、左側の液面の上昇はとまります。
この左側の液面と右側の液面の高さの差に相当する圧力を、浸透圧といいます。
浸透圧の単位
- 容量モル浸透圧濃度(mOsm/L)
- 重量モル浸透圧濃度(mOsm/kgH2O)
浸透圧の単位には、容量モル浸透圧濃度(mOsm/L)と重量モル浸透圧濃度(mOsm/kgH2O)の2つがあります。
それぞれの浸透圧の単位は同じ意味で、水1L(1kg)中に存在する粒子数(mol数)を表しています。
浸透圧の仕組みをさらにわかりやすく解説します
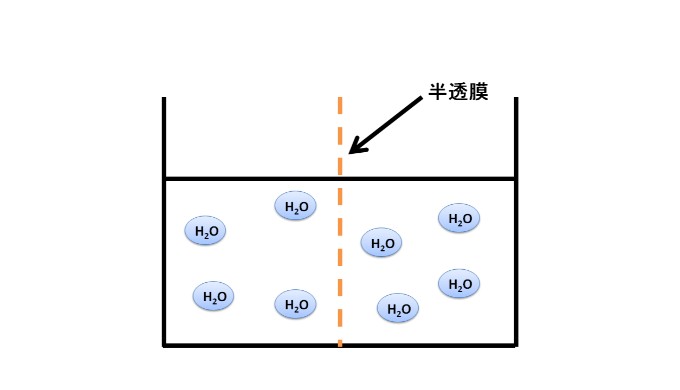
ここではもう少し、浸透圧のメカニズムについて深掘りしていきます。
まず、上の図のように、半透膜(水:H20しか通らない膜)で仕切られた純粋(H20)を用意します。
水の中にブドウ糖を投入【ブドウ糖の拡散】
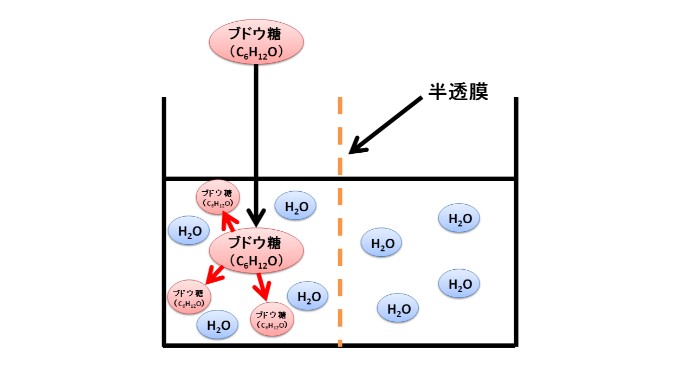
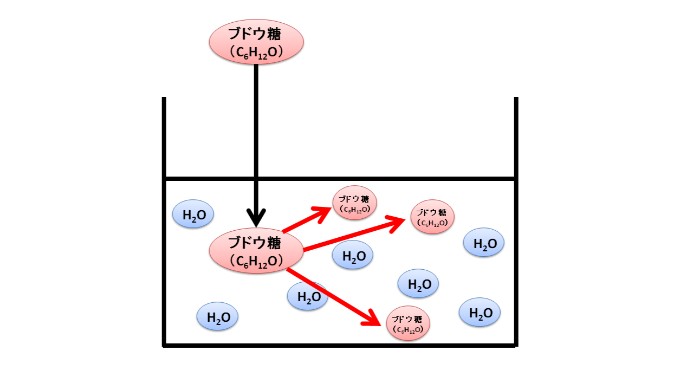
左側の溶液に、ブドウ糖(C6H12O6)をいれます。
ブドウ糖は、半透膜をとおることができないため、左側の溶液内だけで拡散します。
そうすると、左側の溶液と右側の溶液で、ブドウ糖の濃度に違いが出てきます(当たり前ですが、右側の溶液のブドウ糖の濃度はゼロです)。
半透膜をとおって、水が移動する【水の浸透】
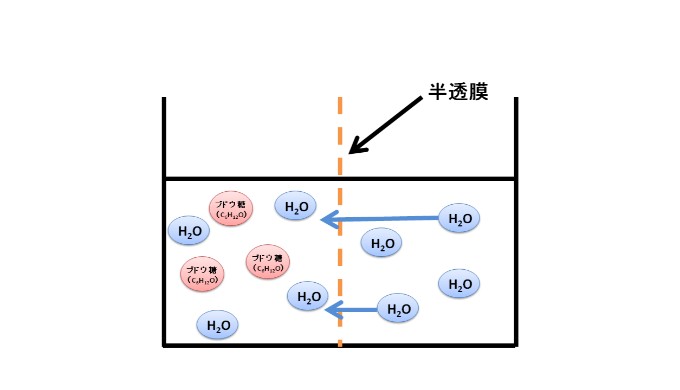
左側の溶液のほうが、ブドウ糖の濃度が濃いです。
ですので、左側の溶液を薄めて、全体の濃度を均一にしようと水分子(H20)の浸透(≒拡散)が起こります。
ようするに、右側の水分子(H20)が左側に移動(浸透≒拡散)します。
この半透膜を介した水の拡散のことを、特に浸透と一般的にいいます。
そういう意味で、拡散と浸透は、本質的には同じ意味です。
左側の溶液の液面が上がる
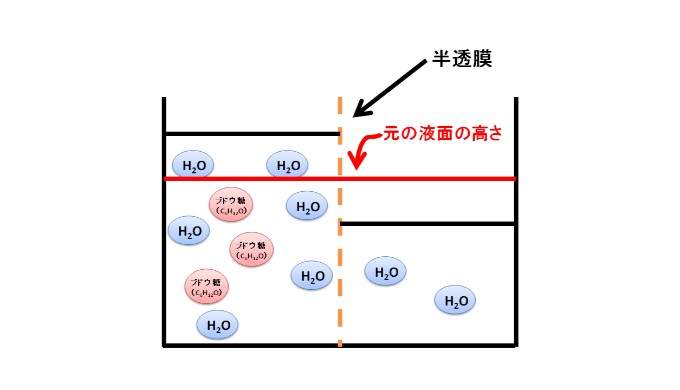
右側の水分子(H20)が左側に移動(浸透≒拡散)した結果、左側の溶液の液面が上がります。
理想的には、溶液全体の濃度を均一にするためには、右側の水が左側にすべて移動しますが、実際にはそうはなりません。
理由は重力の影響があるからです。
ですので、左側の液面と右側の液面の差に相当する圧力が水を押し戻します。
そのため、ある一定のところで、左側の液面の上昇はとまります。
この右側の液面と左側の液面の高さの差に相当する圧力を浸透圧といいます。
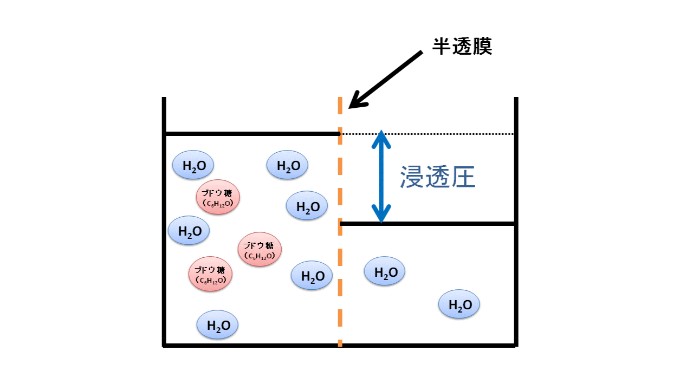
今回の場合でいうと、ブドウ糖は半透膜を通ることができません。そのため、右側の水は、左側の溶液を薄めようと、左側に浸透していきました。
その結果、浸透(半透膜を介した水の拡散)が生じました。
つまり、半透膜を通ることができない物質(今回のケースでは、ブドウ糖)というのは、水の移動(浸透、浸透圧)を引き起こすということです。
補足:左の溶液に圧力を加えて、液面を水平にするときに必要な圧力も浸透圧と同じです
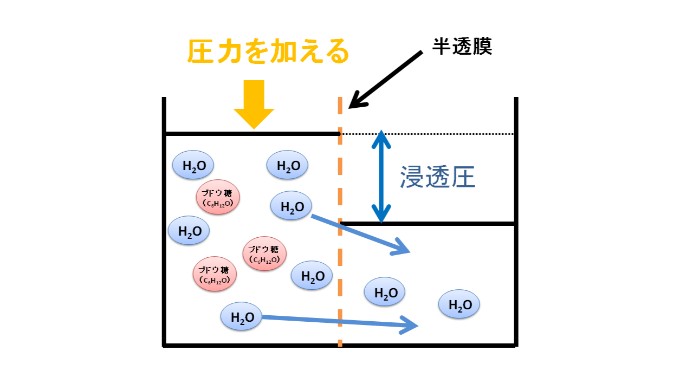
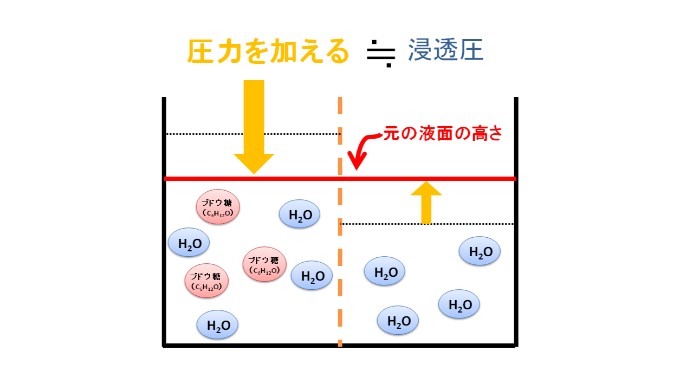
ちなみに、左側の溶液と右側の溶液の液面は、圧力を加えることで元の液面の高さに戻すことができます。
この圧力も、浸透圧と同じことになります。
まとめ:浸透圧とは?

上の図のように、半透膜を通過できない分子(例:ブドウ糖)があると、半透膜を通過できる分子(例:水)は、拡散によって全体の濃度を均一にしようとします。
その結果、水分子は半透膜をとおって、左側の溶液に移動するので、左側の溶液の液面が上昇します。
しかし、左側の液面と右側の液面の差に相当する圧力が水を押し戻す力が発生します。そのため、ある一定のところで、左側の液面の上昇はとまります。
この左側の液面と右側の液面の高さの差に相当する圧力を、浸透圧といいます。
大事なことは、半透膜を通ることができない物質(今回のケースでは、ブドウ糖)というのは、水の移動(浸透、浸透圧)を引き起こすということです。
というわけで、今回は浸透圧についてわかりやすく解説しました。少しでも参考になれば幸いです。
<注意事項> 本ブログに掲載されている情報の正確性については万全を期しておりますが、掲載された情報に基づく判断については利用者の責任のもとに行うこととし、本ブログの管理人は一切責任を負わないものとします。 本ブログは、予告なしに内容が変わる(変更・削除等)ことがあります。