血漿交換(PE)の基本から、プラズマフローOP-05の特徴、TMP60mmHgを超えてはいけない理由まで、新人看護師・臨床工学技士向けにわかりやすく解説します。
目次
血漿交換(PE)の基本|目的としくみ
- 血漿交換(PE)は「血液中の液体部分(血漿)を丸ごと入れ替える治療」です。
- 透析では除去できない大きなタンパク質(自己抗体・免疫複合体・異常タンパク)を狙って除去します。
- OP-05はIgG・アルブミンもほぼ全て透過する膜であり、選択的ではありません。
- QfはQbの30%以下、TMP≦60 mmHg以下で管理。
血液は「血球(細胞成分)」と「血漿(液体成分)」でできています。血漿交換は、このうち血漿だけを分離して捨て、補充液(アルブミン製剤またはFFP)を入れ替える治療です。
透析との決定的な違い
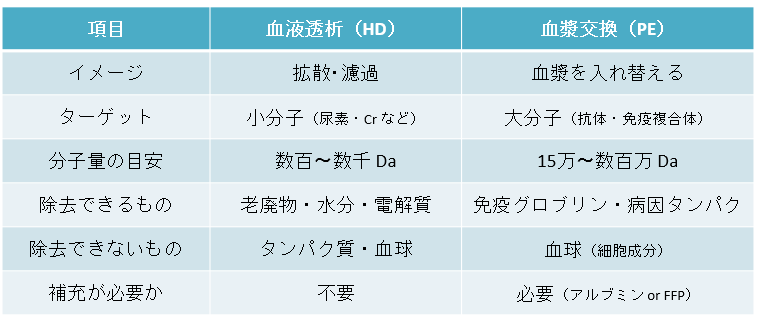
透析(HD)は尿素・電解質のような小分子を除去しますが、血漿交換ではIgG・免疫複合体・異常タンパクなど、透析膜では絶対に抜けない巨大分子を除去できます。
血漿交換の主なターゲット
- 自己抗体(IgG・IgM):MG、GBS、ANCA血管炎
- 免疫複合体:SLE、クリオグロブリン血症
- タンパク結合毒素:劇症肝炎、薬物中毒の一部
- 異常タンパク:マクログロブリン血症など
血漿を捨てるため、凝固因子や栄養素も同時に失われる点がポイントです。
プラズマフローOP-05|「血漿成分をほぼ全量抜く」膜
OP-05の特徴
- 膜孔径:0.1 μm(精密濾過膜)
- 血球は通さず、血漿のみを分離
- ふるい係数:アルブミン 0.97、IgG 0.97 → ほぼ全量透過
- 最高使用限外濾過圧:8 kPa(60 mmHg):添付文書に明記
- QfはQbの30%以下:TMP上昇と溶血の防止
OP-05は抗体だけを“選択的に”落とすものではありません。血漿タンパク全体を落とす治療です。
OP-05のモニタリング|TMPは絶対に60 mmHgを超えない
TMPとは
TMP(Transmembrane Pressure)は、血液側と血漿側の圧差=膜にかかる押し出し圧です。
なぜTMP60mmHg以下が絶対なのか
60 mmHgは「臨界膜間圧」の目安であり、これを超えると赤血球損傷・膜閉塞が急増します。
① 溶血を防ぐため|赤血球への「せん断応力」
OP-05の膜孔径(0.1 μm)は血漿だけを通し、赤血球(7〜8μm)は通しません。このときTMPが高すぎると、赤血球が膜孔に押し付けられ、すり切られるような力(せん断応力)がかかります。
赤血球は変形能を持ちますが、過度な圧力では細胞膜が破壊され、
- 遊離Hb上昇
- K上昇
- 血漿の赤色化(機械的溶血)
といった典型的な溶血所見を来します。
複数の膜型TPE(mTPE)の報告では、TMPが50〜60mmHg付近まで上昇した症例で、フィルタ凝固や回路トラブルが有意に多いことが示されています。
● Elali 2021(mTPE 135回)
→ 回路凝固群:平均 TMP 57.48 mmHg
→ 正常群:44.43 mmHg
● Gashti 2018(mTPE 998回)
→ トラブル群:54.5 mmHg
→ 正常群:43.7 mmHg
つまり、TMP50〜60mmHgが“赤信号ゾーン”。
② 膜の詰まり(ファウリング)を防ぐため|濃度分極とゲル層形成
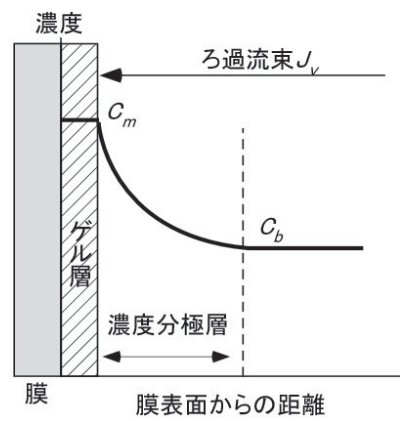
TMPが高い状態では、血漿成分(特にタンパク質)が膜面に押し付けられ、
- 濃度分極層(タンパク濃縮層の形成)
- ゲル層形成(膜表面が粘稠なタンパク層で覆われる)
が急速に進みます。
こうなると:
- 血漿が引けない → Qfが落ちる
- TMPがさらに上昇する
- 治療が早期終了する
という悪循環になります。
脂質異常症患者での報告では「低いTMPほど血清脂質の除去効率が高い」ことも示され、TMP上昇=膜閉塞のサインであることが確認されています。
③ 添付文書の仕様上の上限|8 kPa(60 mmHg)
プラズマフローOPシリーズでは、添付文書に
最高使用限外濾過圧:8 kPa(=60 mmHg)
と明記されています。
これは「ここを超えると膜の耐久性が保証されない」ことを意味し、臨床的にも守る必要があります。
現時点では、赤血球が「どの圧力差(mmHg)で必ず溶血するか」を示した臨床試験データは存在しません。
ただし、実験モデルでは 30〜100 Pa(約0.23〜0.75 mmHg) を超えるせん断応力にさらされると、赤血球の変形悪化や損傷が急増するという報告があります。
一方で、プラズマ分離器の TMP は 血液側と血漿側の圧差=“膜にかかる押し出し圧” であり、せん断応力(Pa)とは物理的性質が異なります。TMP をそのまま Pa のように扱うことはできませんが、TMP が高くなるほど膜面付近の流速勾配や赤血球の圧迫・変形ストレスが増え、結果として“機械的溶血が起こりやすくなることがわかっています。
このため、膜型血漿分離器の運転では、メーカー仕様(最高使用限外濾過圧 8 kPa=約60 mmHg)や、膜の耐久性・溶血リスク・ファウリング(目詰まり)など複数のリスクを総合して、
「TMP=60 mmHg以下」を安全運転の経験的な指標
として用いることが一般的です。
TMPが上がったときはどうする?
- Qfを下げる(最優先)
- Qbが低下していないか確認(脱血不良)
- Ht高値なら補液を検討
- 回路・膜の交換を考える
60mmHgを超えた状態で運転を続けるのは、溶血と膜破損のリスクがあり危険です。
まとめ|OP-05で行う血漿交換のポイント
血漿交換(PE)は、透析では除去できない大きなタンパク質(自己抗体・免疫複合体など)を下げるための治療です。プラズマフローOP-05はアルブミンやIgGもほぼ全量透過する膜であり、治療効果が高い一方、膜閉塞や溶血を防ぐための安全運転が欠かせません。
- OP-05は「血漿を丸ごと入れ替える」治療であり選択性はほぼ無い。
- Qf/Qbは30%以下:血液側への負荷とTMP上昇を防ぐ。
- TMPは60mmHg以下:膜閉塞(濃度分極・ゲル層形成)と機械的溶血を防ぐための重要な上限。
- 置換量は1.0〜1.5PV:病因物質の除去率を安定させる標準的な量。
- 置換液は疾患で使い分ける:TTPはFFP、自己免疫疾患はアルブミンが基本。
- 溶血リスクは「せん断応力(Pa)」と関連しており、TMPが高い運転は赤血球損傷の誘因となる。
- フィルタ凝固や治療中断はTMPの上昇が前触れになるため、圧変化の観察が最重要。
OP-05の血漿交換は、設定値・圧モニタ・置換量の3点を押さえることで安全性が大きく高まります。TMP上昇を早期に察知して介入することが、治療を最後まで安定して継続するための鍵です。